- Home
- Bloguri
- Descopera produse
- Vitamine, minerale si suplimente
- Cuplu si sex
- Produse de slabit
- Medicamente
- Special la Catena
- Tehnico - medicale
- Frumusete si ingrijire
- Mama si copilul
- Acnee
- Diverse
- Nutritie sanatoasa
- Produse naturiste
- Medicamente fertilitate
- Produse BIO
- Idei de cadouri
- NOU la Catena
- Alimente cu destinatie speciala
- Ce Oftapic ti se potriveste
- Adora – Adorabili din prima clipa
- oferte
- card club
- prospecte
- Catalogul lunii
Broncho-Vaxom 3,5mg x 30 caps
Broncho-Vaxom 3,5mg x 30 caps - Catena
O caspula contine: liofilizat de lizate bacteriene de Haemophilus influenzae, Diplococcus pneumoniae, Klebsiella pneumoniae si ozaenae, Staphylococcus aureus, Streptococcus pyogenes si viridans, Neisseria catarrhalis 7 mg si excipienti: continutul capsulei - galat de propil anhidru, glutamat monosodic, amidon pregelatinizat, stearat de magneziu, manitol; capsula - indigotina
(E 132), dioxid de titan (E 171), gelatina; cerneala de inscriptionare - Shellac, carbune vegetal (E 153).
Producator: OM PHARMA -ELVETIA
*Pentru pret te asteptam in cea mai apropiata farmacie Catena
CELE MAI RECENTE ARTICOLE
-
Tranzitia de la alaptat la biberon: sfaturi si trucuri pentru o trecere linaTimp de citire: 6 minute, 15 secunde1 aprilie 2025
Fiecare etapa din viata bebelusului vine cu provocari noi pentru parinti, iar una dintre ele este tranzitia de la alaptat la biberon. Fie ca este vorba despre intoarcerea mamei la serviciu, despre nevoia…
-
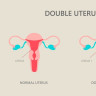
Uter didelf (uter dublu)Timp de citire: 5 minute, 42 secunde1 aprilie 2025
Uterul didelf, cunoscut si sub denumirea de uter dublu, este o anomalie congenitala rara a sistemului reproducator feminin, in care o femeie are doua cavitati uterine separate, fiecare cu propriul sau…
-
Sindromul Rapp-HodgkinTimp de citire: 4 minute, 58 secunde1 aprilie 2025
Sindromul Rapp-Hodgkin este o tulburare genetica rara care afecteaza in primul rand dezvoltarea anumitor structuri ale corpului, in special dintii, parul si unghiile. Poate avea un impact semnificativ…
-
Valve cardiace: functionare, afectiuni si tratamentTimp de citire: 6 minute, 8 secunde1 aprilie 2025
Functionarea normala a intregului sistem cardiovascular depinde in buna masura si de niste structuri anatomice situate in interiorul inimii, cunoscute sub denumirea de valve cardiace. Exista patru astfel…