- Home
- Bloguri
- Descopera produse
- Vitamine, minerale si suplimente
- Cuplu si sex
- Produse de slabit
- Medicamente
- Special la Catena
- Tehnico - medicale
- Frumusete si ingrijire
- Mama si copilul
- Acnee
- Diverse
- Nutritie sanatoasa
- Produse naturiste
- Medicamente fertilitate
- Produse BIO
- Idei de cadouri
- NOU la Catena
- Alimente cu destinatie speciala
- Ce Oftapic ti se potriveste
- Adora – Adorabili din prima clipa
- oferte
- card club
- prospecte
- Catalogul lunii
Buscopan 10 mg x 20 drajeuri
Buscopan 10 mg x 20 drajeuri - Catena
Buscopan este un medicament utilizat pentru ameliorarea contractiilor spastice ale muschilor netezi de la nivelul tractului gastro-intestinal si tractului genitourinar (in stomac, intestine, tract biliar si urinar). De exemplu, Buscopan este recomandat persoanelor care se confrunta cu colici biliare sau renale, spasme gastro-intestinale de diverse origini, sindrom de intestin iritabil sau dureri din timpul ciclului menstrual.
Compozitie:
- Substanta activa este bromura de butilscopolamina. Fiecare drajeu contine bromura de butilscopolamina 10 mg.
- Buscopan contine si alte substante, cum ar fi: hidrogenofosfat de calciu anhidru, amidon de porumb uscat, amidon de porumb solubil, dioxid de siliciu coloidal anhidru, acid tartric, acid stearic, povidona, zahar, talc, guma arabica pulbere, dioxid de titan (E 171), macrogol 6000, ceara alba, ceara Carnauba.
Mod de administrare:
Buscopan se administreaza pe cale orala.
- Adulti: doza recomandata este de 2 drajeuri Buscopan, de 4 ori pe zi. Pentru ameliorarea simptomelor sindromului de colon iritabil, doza initiala recomandata este de un drajeu Buscopan, de 3 ori pe zi. Daca este necesar, aceasta doza poate fi crescuta la 2 drajeuri Buscopan, de 4 ori pe zi.
- Copii cu varsta cuprinsa intre 6 si 12 ani: doza recomandata este de un drajeu Buscopan, de 3 ori pe zi.
Drajeurile se administreaza intregi, cu o cantitate suficienta de lichid.
Contraindicatii:
Nu utilizati Buscopan daca sunteti alergic (hipersensibil) la bromura de butilscopolamina sau la oricare dintre celelalte componente ale acestui medicament.
Precautii:
Adresati-va medicului sau farmacistului inainte sa utilizati Buscopan.
Sarcina, alaptarea si fertilitatea:
Daca sunteti gravida sau alaptati, daca banuiti ati putea fi gravida sau intentionati sa ramaneti gravida, adresati-va medicului sau farmacistului pentru recomandari inainte de a lua acest medicament.
Ca masura de precautie, este de preferat sa evitati sa utilizati Buscopan in timpul sarcinii si alaptarii.
Producator: SANOFI
*Pentru pret te asteptam in cea mai apropiata farmacie Catena
CELE MAI RECENTE ARTICOLE
-
Xantopsie – cauze, simptome si tratamentTimp de citire: 6 minute, 59 secunde2 aprilie 2025
Xantopsia este o tulburare de vedere in care pacientii percep obiectele in nuante de galben sau auriu. Aceasta afectiune poate fi asociata si cu alte tulburari oculare, cum ar fi cataracta, degenerescenta…
-
Calmarea tusei seci la copii: ghid complet pentru parintiTimp de citire: 6 minute, 0 secunde2 aprilie 2025
Tusea seaca este o problema comuna de sanatate in randul copiilor, de obicei mai mult suparatoare decat grava. Cu toate acestea, este firesc ca parintii sa se preocupe de gasirea unor remedii pentru calmarea…
-
Tranzitia de la alaptat la biberon: sfaturi si trucuri pentru o trecere linaTimp de citire: 6 minute, 15 secunde1 aprilie 2025
Fiecare etapa din viata bebelusului vine cu provocari noi pentru parinti, iar una dintre ele este tranzitia de la alaptat la biberon. Fie ca este vorba despre intoarcerea mamei la serviciu, despre nevoia…
-
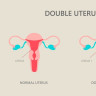
Uter didelf (uter dublu)Timp de citire: 5 minute, 42 secunde1 aprilie 2025
Uterul didelf, cunoscut si sub denumirea de uter dublu, este o anomalie congenitala rara a sistemului reproducator feminin, in care o femeie are doua cavitati uterine separate, fiecare cu propriul sau…